
Potencial de Membrana
Las membranas celulares. Gradiente iónico y potencial eléctrico de membrana. Células excitables. Movimiento de iones a través de membranas biológicas. Medida experimental del potencial eléctrico de una membrana. Cálculo del Potencial Eléctrico de Membrana. Potencial de reposo: Generación por Canales de reposo.
Potencial de acción. Las propiedades eléctricas pasivas de la membrana del axón. Modelo de Hodgkin y Huxley: cambios de conductancia durante la actividad.
La membrana celular es permeable a algunos gases y a algunas pequeñas moléculas polares no cargadas, es ligeramente permeable al agua y esencialmente impermeable a la mayoría de moléculas solubles en agua. Por tanto, se requiere la presencia de ciertas proteínas para transportar moléculas polares e iones a través de las membranas celulares. Dichas proteínas permiten a estas moléculas cruzar la membrana sin interaccionar directamente con su interior hidrofóbico.

Tipos fundamentales de proteínas transportadoras de membrana
Estos últimos transportan agua y tipos específicos de iones a favor de su gradiente de concentración. Forman un paso de proteína a través de la membrana por el cual se pueden mover simultáneamente un múltiple número de moléculas a gran velocidad. Estos canales juegan un papel fundamental en el funcionamiento de células nerviosas y en la transmisión de impulsos nerviosos.
GRADIENTE IÓNICO Y POTENCIAL ELÉCTRICO DE MEMBRANA. CÉLULAS EXCITABLES
La membrana celular es el orgánulo que hace posible mantener una composición iónica del medio intracelular completamente distinta a la del extracelular. Esta diferencia en concentración se mantiene por la presencia de bombas, transportadores y canales iónicos. La composición iónica del citosol difiere ampliamente de aquella del fluido extracelular.
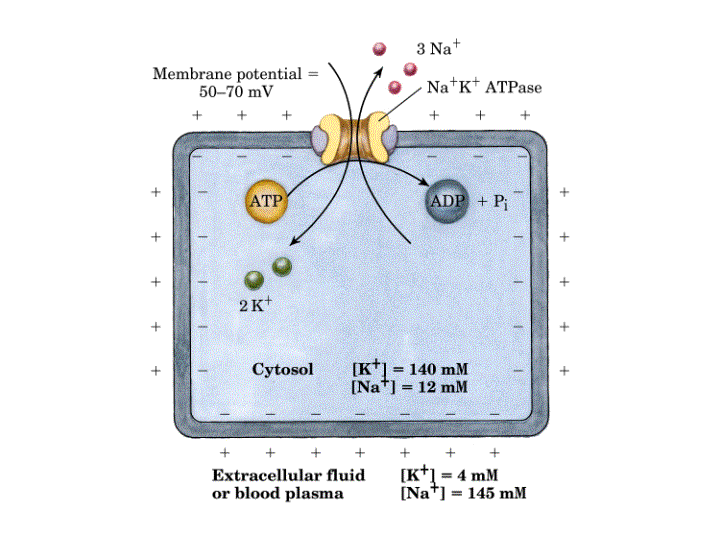
Así, en casi todas las células, a pH 7, la concentración citosólica de K+ es mucho mas alta que la de Na+y Ca2+. Por ejemplo, [K+] < 20-40 veces en sangre que en las células. Por otro lado, la [Ca2+] es mucho menor en el interior celular que en el medio extracelular. Las bombas iónicas, fundamentalmente la bomba de Na+/K+, son las que generan y mantienen este gradiente de concentración iónica consumiendo ATP.
La membrana plasmática contiene canales proteicos que permiten a los principales iones celulares (Na+, K+, Ca2+ y Cl-) cruzar la membrana a favor de su gradiente de concentración a distintas velocidades. Los gradientes de concentración de iones y el movimiento de iones a través de la membrana crean una diferencia de potencial eléctrico entre el interior y el exterior de la membrana celular. A esta diferencia de potencial eléctrico se la denomina Potencial de Membrana (DY). En la mayor parte de las células el valor de dicho potencial suele ser de unos -60 o -70 mV (el signo negativo indica que el interior de la célula presenta carga negativa respecto al exterior) y se debe únicamente a un ligero exceso de cationes, de tan solo ppm, en el exterior celular.

Teniendo en cuenta este valor de potencia de membranal, -70 mV, y que la membrana plasmática tiene un grosor de 3.5 nm. El gradiente de voltaje que se genera en esta membrana resulta de 0.07 V por 3.5x10-7 cm = 200000 V/cm. Por tanto, la membrana plasmática, como todas las membranas biológicas, se comporta como un artilugio eléctrico que recibe el nombre de condensador (fina hoja de material no-conductor (interior hidrofóbico) rodeado a ambos lados de material eléctricamente conductor (cabezas polares e iones del medio acuoso)). De esta forma la membrana es un almacén de carga eléctrica.
Esta diferencia de gradientes y el potencial eléctrico a través de la membrana dirigen muchos procesos biológicos. Así, por ejemplo, la apertura y cierre de canales de Na+, K+, Ca2+ y Cl-, es sencial para la conducción de impulsos nerviosos a través de los axones de células nerviosas y, el aumento en la concentración de Ca2+, importante señal reguladora (contracción muscular, secreción de hormonas).
POTENCIAL DE REPOSO: GENERACIÓN POR CANALES DE REPOSO DE K+
Hemos dicho que el potencial de membrana través de la membrana plasmática de las células animales se encuentra en torno a -70 mV, a esta diferencia de potencial se le denomina Potencial de Reposo. La cara citosólica es negativa con respecto a la cara exoplásmica. Esto sucede porque las membranas contienen muchos canales de K+ abiertos permanentemente pero muy pocos de Na+ o Ca2+. El mayor movimiento de iones a través de la membrana es de K+, y de dentro a fuera, generando un exceso de cargas negativas en el interior y un exceso de positivas en el exterior. Esto determina el potencial de membrana negativo del interior. Este potencial de membranaes rrelativamente estable y contrasta con los cambios repentinos que ocurren en las células excitables durante su actividad y por ello se le llama potencial de reposo.
| La ATPasa Na+/K+, genera un gradiente de concentración de K+, y es el movimiento de este ion, a través de los canales de K+ de reposo, desde el citosol al exterior celular a favor de su gradiente de concentración el que genera el potencial de membrana negativo en el interior. Por tanto, son los canales de K+ de reposo, que están siempre abiertos, los que generan el potencial de reposo. |  |
Sin embargo, en las células la situación es un poco más complicada, ya que también hay canales para otros iones permanentemente abiertos en condiciones de reposo (canales de reposo). Consideraremos sólo Na+, K+ y Cl-, ya que aunque en la célula también hay otros iones, pocos canales los admiten.
Para calcular el potencial de membrana en función de las concentraciones de diferentes iones se hace preciso definir la constante de permeabilidad, P, para cada ion. Esta es una medida de la facilidad con la cual un ion puede cruzar una unidad de área (1 cm) de membrana impulsado por una diferencia de concentración 1 M. Es proporcional al número de canales iónicos abiertos y al número de iones que cada canal puede conducir por minuto. Unidades cm/s. La permeabilidad no se mide directamente, sino que se suele medir el número de canales abiertos y la conductividad de cada canal.
El potencial de membrana viene dado entonces por la ecuación de Goldman-Hodgkin-Katz

MEDIDA EXPERIMENTAL DEL POTENCIAL ELÉCTRICO DE MEMBRANA
El potencial a través de la membrana plasmática de células suficientemente grandes puede medirse con un microelectrodo insertado en la célula y un electrodo de referencia colocado en el fluido extracelular. Ambos se conecta a un voltímetro capaz de medir pequeñas diferencias de potencial.
El potencial a través de la superficie de la membrana de la mayoría de las células animales normalmente no varia con el tiempo. Sin embargo, las neuronas y células musculares, células activamente eléctricas, llevan a cabo cambios controlados de sus potenciales de membrana. Estos cambios en potencial pueden ser introducidos también artificialmente con objeto de estudiar dichas membranas.
MOVIMIENTO DE IONES A TRAVÉS DE MEMBRANAS BIOLÓGICAS
La velocidad y extensión del transporte iónico a través de las membranas resulta influenciada no únicamente por la concentración de iones a ambos lados de la membrana, sino también por el potencial electroquímico que existe a través de la membrana. Este potencial se encuentra presente en todo tipo de células, pero ha sido estudiado en mayor detalle en células excitables, como fibras musculares esqueléticas y neuronas.
El movimiento de iones a través de membranas selectivamente permeables esta gobernado por dos fuerzas que pueden actuar en la misma dirección o en opuesta:
*potencial eléctrico de membrana
*gradiente de concentración iónico

el movimiento de iones Na+ al interior de la célula se utiliza como energía para el transporte de varios iones y de pequeñas moléculas catalizado por proteínas simporte y antiporte.
POTENCIAL DE ACCIÓN. LAS PROPIEDADES ELÉCTRICAS PASIVAS DE LA MEMBRANA DEL AXÓN. MODELO DE HODGKING Y HUXLEY. CAMBIOS DE CONDUCTANCIA DURANTE LA ACTIVIDAD.
Determinadas células, como por ejemplo las neuronas y las células musculares son eléctricamente activas, y sufren cambios repentinos en el potencial de sus membranas que se aleja momentáneamente del valor estable del potencial de reposo. A esta repentina alteración del potencial de membrana se le denomina potencial de acción o impulso nervioso.

El potencial de acción (impulso nervioso) es un señal eléctrica producida por el flujo de iones que circulan a través de la membrana plasmática de una neurona. El potencial de acción, o impulso nervioso, se produce cuando el potencial de membrana se despolariza por encima de un umbral crítico (-60 a -40 mV). En un msg el potencial de membrana se vuelve positivo, +40 mV, y luego vuelve a ser negativo. Esta despolarización amplificada se propaga a las regiones adyacentes de la membrana plasmática permitiendo al potencial de acción viajar a lo largo de los axones de las células nerviosas como señales eléctricas, resultando en una rápida transmisión de los impulsos nerviosos a grandes distancias.
En el descubrimiento y estudio de la naturaleza de este potencial de acción los axones de los calamares gigantes han sido fundamentales, ya que son de un tamaño considerable (diámetro 0.2-1 mm; 5-10 cm largo) y permiten que los electrodos puedan ser fácilmente insertados en el citosol para detectar pequeños cambios de potencial.
Hodgkin y Huxley demostraron que el potencial de acción se debe a cambios grandes y transitorios de la permeabilidad de la membrana del axón respecto a los iones Na+ y K+. Mediante el estudio del cambio de permiabilidad de estos iones establecieron la existencia de dos tipos de conductos o canales sensibles al voltaje (canales iónicos dependientes de voltaje), y concluyeron que el proceso de generación de un potencial de acción debía componerse de las siguientes etapas:
Durante todo este proceso, sólo una pequeña proporción de iones sodio y potasio (1 ppm) fluye a través de la membrana. Por tanto, el potencial de acción es es un método muy eficaz de enviar señales a grandes distancias.
Hodgkin y Huxley establecieron tres cuestiones clave en este mecanismo cuya resolucíon pasa por el estudio de la relación estructura-función de estos canales.

Bibliografía
|
Página creada y mantenida por Milagros Medina
Última modificación 20 de Marzo de 2007